


《人教版化学选修5化学《醇-酚》PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为1.59 MB,总共有33页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 33页
- 1.59 MB
- VIP模板
- ppt
- 数字产品不支持退货
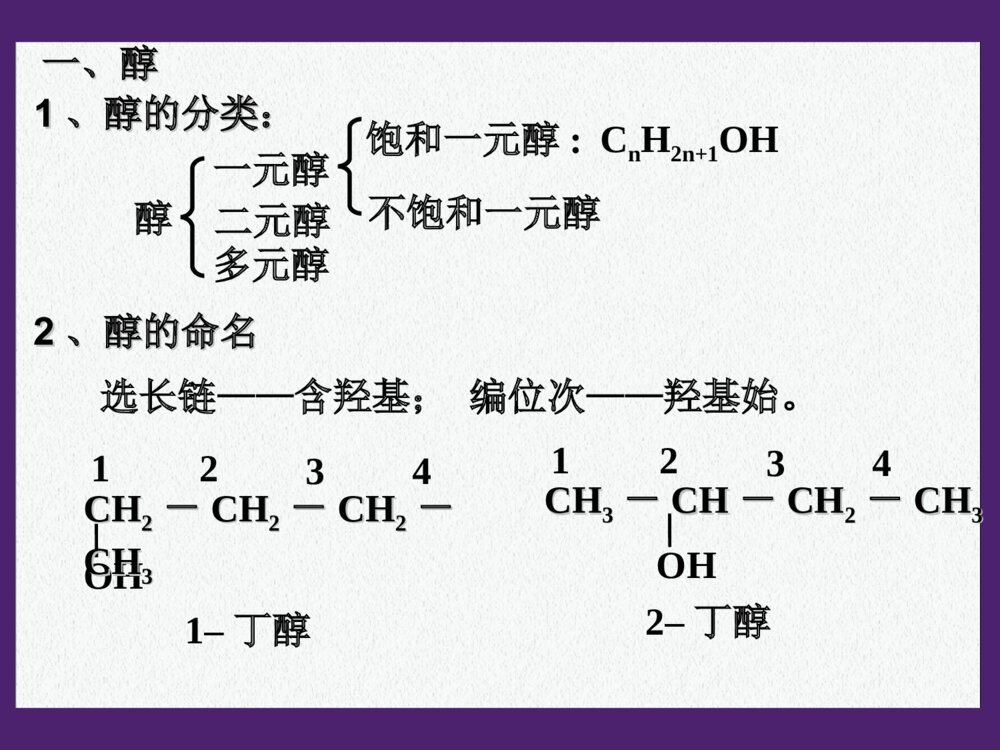
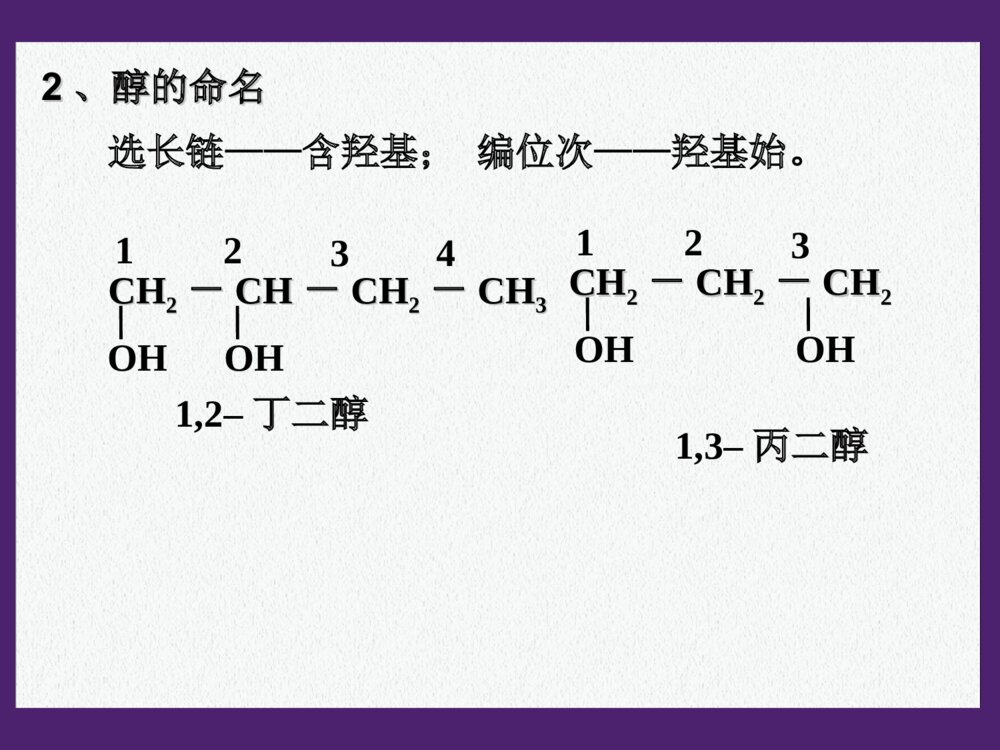
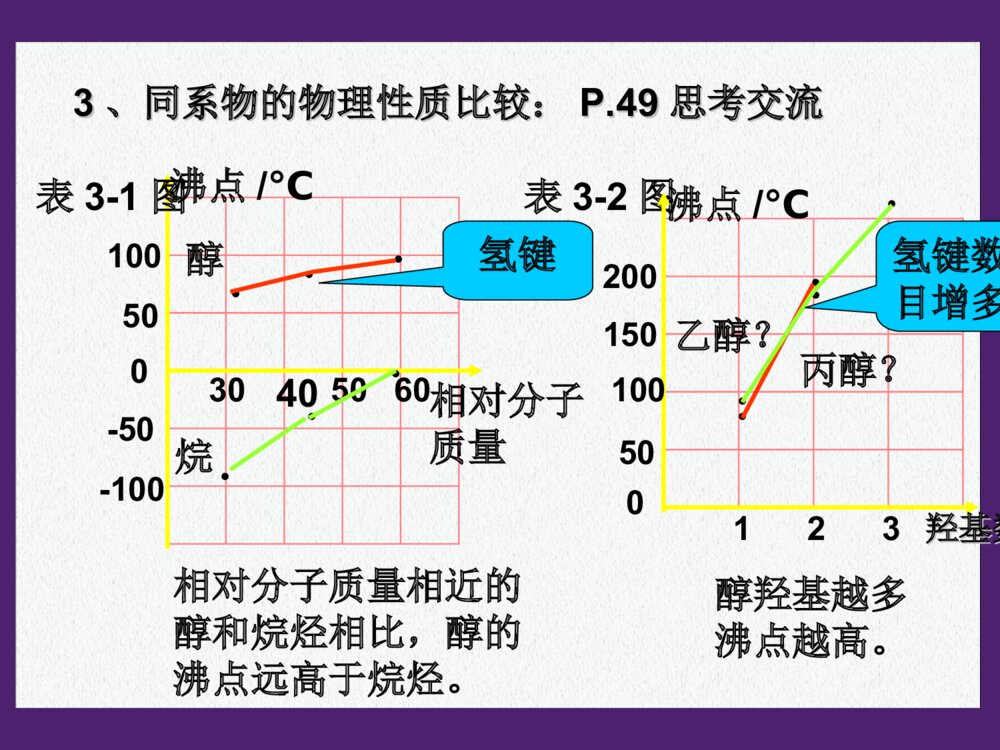
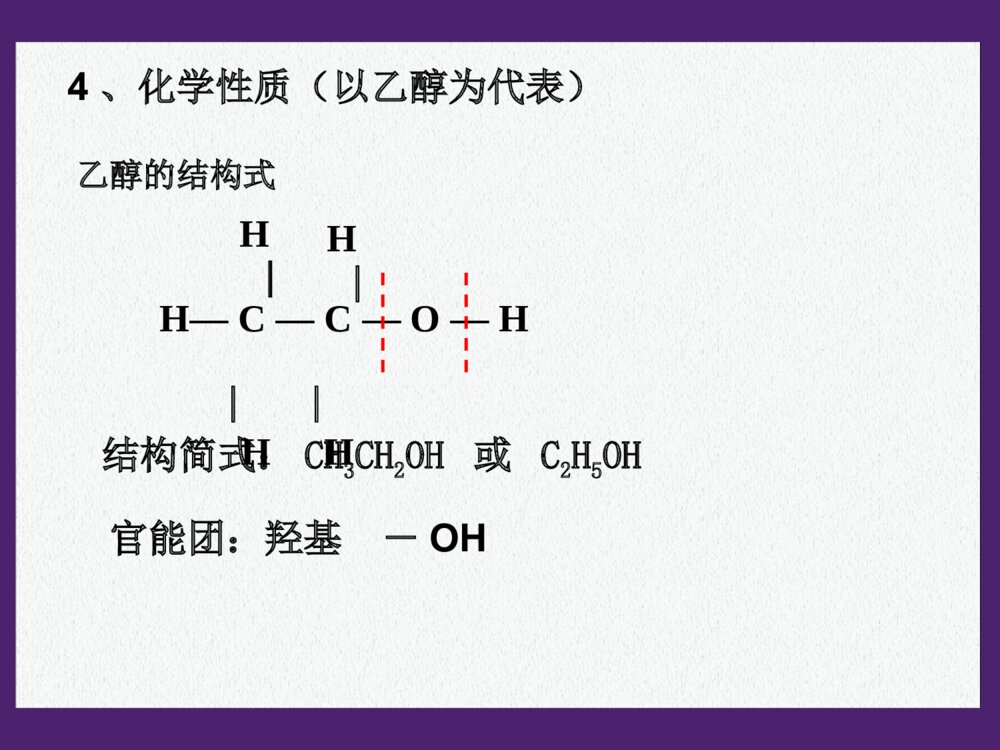
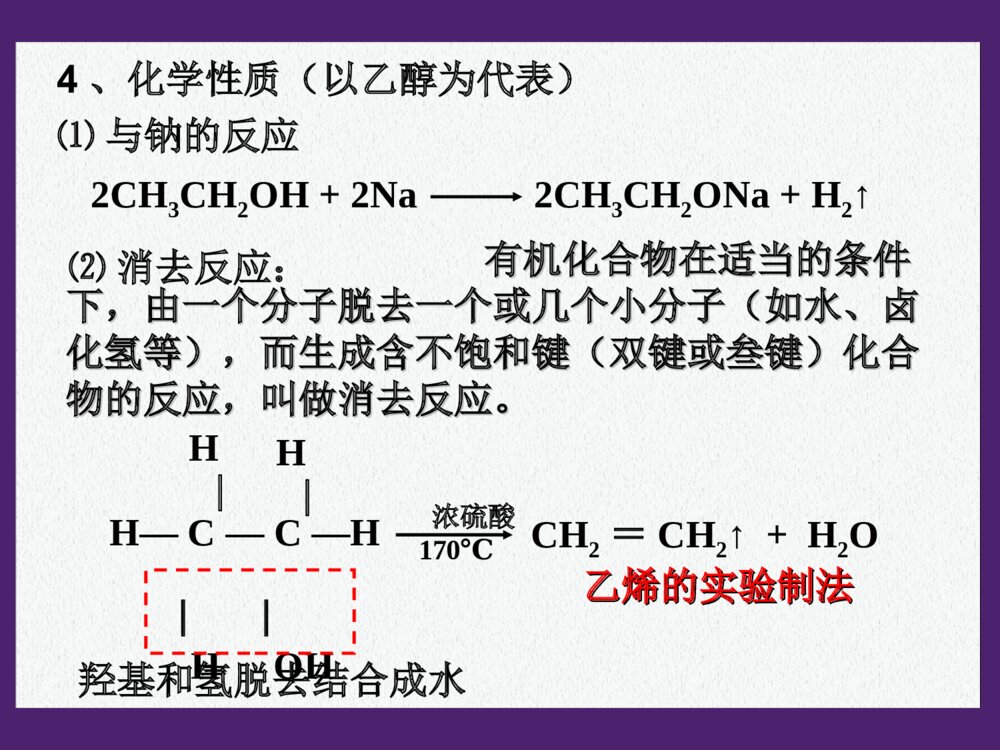
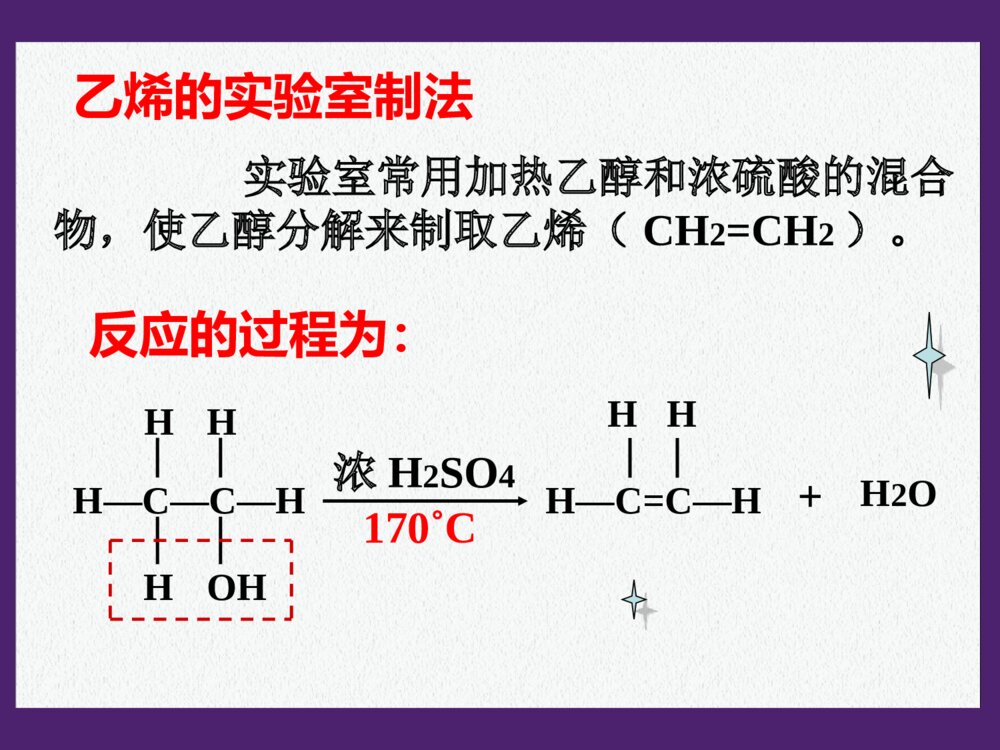
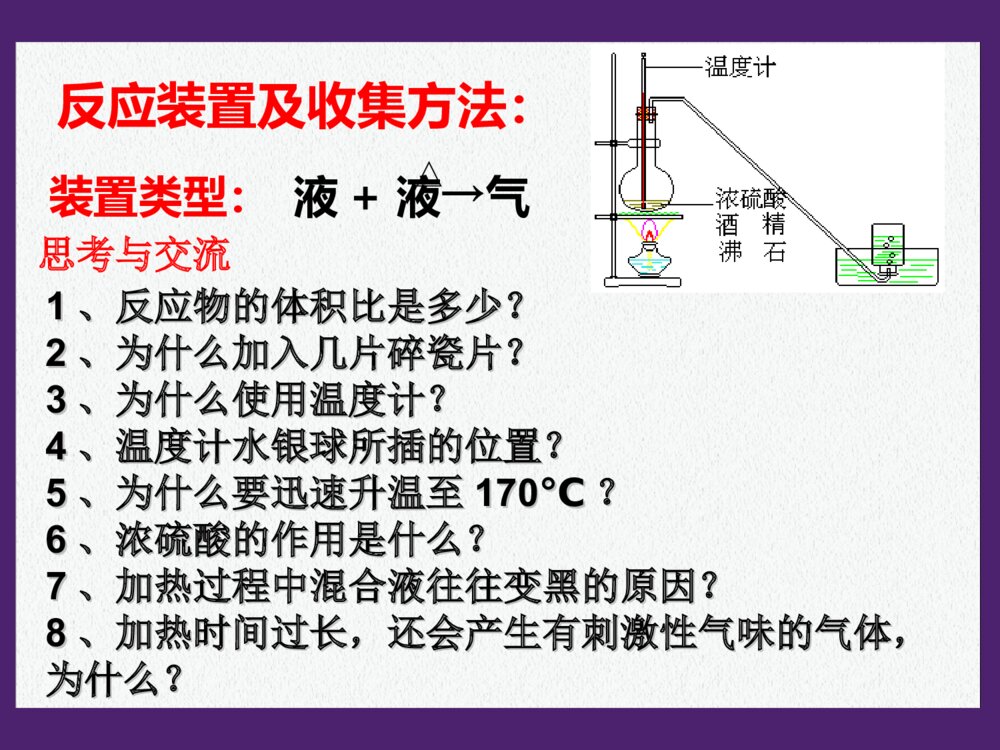
第三章烃的含氧衍生物第一节醇酚1、什么叫烃的含氧衍生物?2、烃的含氧衍生物包括哪些种类?3、如果烃分子中的氢原子被-OH取代产物属于哪类物质?烃的含氧衍生物的概念:烃分子中的氢原子被含有氧的原子团取代得到的化合物称为烃的含氧衍生物。含羟基化合物醇酚羟基与烃基或苯环侧链上的碳原子相连的化合物。分子中羟基与苯环直接相连而形成的化合物。烃的含氧衍生物的类别:醇、酚、醛、羧酸和酯等。醇一元醇多元醇饱和一元醇:不饱和一元醇CnH2n+1OH二元醇一、醇一、醇11、醇的分类:、醇的分类:22、醇的命名、醇的命名选长链——含羟基;编位次——羟基始。4321OHCHCH22--CHCH22--CHCH22--CHCH331–丁醇4321OHCHCH33--CHCH--CHCH22--CHCH332–丁醇22、醇的命名、醇的命名选长链——含羟基;编位次——羟基始。43211,2–丁二醇3211,3–丙二醇OHCHCH22--CHCH--CHCH22--CHCH33OHOHCHCH22--CHCH22--CHCH22OH相对分子质量沸点/℃表3-1图050100-50-10030405060表3-2图羟基数羟基数沸点/℃015020010050123●●●●●●●●●●●醇烷乙醇?丙醇?相对分子质量相近的醇和烷烃相比,醇的沸点远高于烷烃。醇羟基越多沸点越高。氢键氢键数目增多33、同系物的物理性质比较:、同系物的物理性质比较:P.49P.49思考交流思考交流结构简式:CH3CH2OH或C2H5OHH—C—C—O—H︳H︳HH︳H︳乙醇的结构式4、化学性质(以乙醇为代表)官能团:羟基-OH4、化学性质(以乙醇为代表)⑴与钠的反应2CH3CH2OH+2Na2CH3CH2ONa+H2↑⑵消去反应:羟基和氢脱去结合成水H—C—C—H︳H︳OHH︳H︳CH2=CH2↑+H2O浓硫酸170℃有机化合物在适当的条件有机化合物在适当的条件下,由一个分子脱去一个或几个小分子(如水、卤下,由一个分子脱去一个或几个小分子(如水、卤化氢等),而生成含不饱和键(双键或叁键)化合化氢等),而生成含不饱和键(双键或叁键)化合物的反应,叫做消去反应。物的反应,叫做消去反应。乙烯的实验制法乙烯的实验制法下列各种醇能否发生消去反应?能发生消下列各种醇能否发生消去反应?能发生消去反应的醇的分子结构特点是什么?去反应的醇的分子结构特点是什么?醇发生消去反应的条件有:醇发生消去反应的条件有:①①连有-连有-OHOH的碳原子周围有碳原子。的碳原子周围有碳原子。②②与连有-与连有-OHOH的碳原子相邻的碳原子上有氢原子。的碳原子相邻的碳原子上有氢原子。思考:CH3OHOHCHCH22--CHCH--CHCH22--CHCH33CH3OHCHCH22--CC--CHCH22--CHCH33CH3CH31、2、3、不能能不能乙烯的实验室制法实验室常用加热乙醇和浓硫酸的混合物,使乙醇分解来制取乙烯(CH2=CH2)。反应的过程为:HHH—C—C—HOHH浓H2SO4H—C=C—HHH+H2O170˚C反应装置及收集方法:装置类型:液+液→气11、反应物的体积比是多少?、反应物的体积比是多少?22、为什么加入几片碎瓷片?、为什么加入几片碎瓷片?33、为什么使用温度计?、为什么使用温度计?44、温度计水银球所插的位置?、温度计水银球所插的位置?55、为什么要迅速升温至、为什么要迅速升温至170℃170℃??66、浓硫酸的作用是什么?、浓硫酸的作用是什么?77、加热过程中混合液往往变黑的原因?、加热过程中混合液往往变黑的原因?88、加热时间过长,还会产生有刺激性气味的气体,、加热时间过长,还会产生有刺激性气味的气体,为什么?为什么?思考与交流(1)浓硫酸与乙醇的体积比为3:1,混合时应将浓硫酸缓缓加入乙醇中并不断搅拌。C2H5OH2C+3H2O浓硫酸C+2H2SO4(浓)==CO2↑+2SO2↑+2H2O△(2)为了防止溶液剧烈沸腾,需要在混合液中加入少量的碎瓷片。(4)对反应温度的要求:170℃以下及170℃以上不能有效脱水,故必须迅速将温度升至170℃并保持恒温。140℃时分子间脱水生成乙醚和水;170℃以上浓硫酸使乙醇脱水而炭化。zxxk(3)用温度计指示反应温度,温度计的水银球在液面以下!(6)气体的净化:NaOHH2SO4可能有哪些杂质?[思考]在实验室里制备的乙烯中常含有SO2,试设计一个实验,检验SO2的存在并验证乙烯的还原性。(5)浓硫酸:催化剂、脱水剂。CH3CH2BrCH3CH2OH反应条件化学键的断裂化学键的生成反应产物学与问学与问溴乙烷和乙醇都能发生消去反应,它们有什么不同?溴乙烷和乙醇都能发生消去反应,它们有什么不同?NaOHNaOH乙醇溶液,乙醇溶液,加热加热浓硫酸,浓硫酸,加热至加热至170℃170℃CC--BrBr、、CC--HH键键CC--OO、、CC--HH键键CHCH22==CHCH22、、NaBrNaBr、、HH22OOCHCH22==CHCH22、、HH22OOCC==CCCC==CC通常情况下,我们把与官能团直接相连的碳通常情况下,我们把与官能团直接相连的碳原子称为原子称为αα碳原子,把与碳原子,把与αα碳原子相连的碳原子称为碳原子相连的碳原子称为ββ碳原子,与碳原子,与ββ碳原子相连的氢原子称为碳原子相连的氢原子称为ββ氢原子。氢原子。例如,例如,2-2-丁醇中存在丁醇中存在11个个αα碳原子和碳原子和22个个ββ碳原子碳原子醇(或卤代烃)发生消去反应时,羟基(或醇(或卤代烃)发生消去反应时,羟基(或卤原子)来自卤原子)来自αα碳原子,氢原子来自碳原子,氢原子来自ββ碳原子。当醇碳原子。当醇(或卤代烃)分子中存在(或卤代烃)分子中存在22个或个或33个个ββ碳原子,且这碳原子,且这些碳原子连有氢原子时,发生消去反应的产物就可能些碳原子连有氢原子时,发生消去反应的产物就可能有多种。有多种。ββ氢与消去反应氢与消去反应OHCHCH33--CHCH--CHCH22--CHCH33ααββββ试写出下列化合物消去H2O后可得到的产物的结构简式(暂不考虑顺反异构)。——CH3OHCH3CH2CH2—C—CH2CH3——CHCH33CHCH33CHCH22CHCH22--CC==CHCHCHCH33——CHCH33CHCH33CHCH22CHCH==CC--CHCH22CHCH33——CHCH22CHCH33CHCH33CHCH22CHCH22--CC==CHCH22①分子间脱水②乙醇与浓氢卤酸的取代反应2CH3CH2OHCH3CH2-O-CH2CH3+H2O140℃浓硫酸CH3CH2-OH+H-Br氧化反应:有机物分子失氢得氧的反应。⑶⑶取代反应取代反应△CH3CH2-Br+H2O2CH3CH2OH+O22CH3CHO+2H2OCu或Ag△⑷氧化反应还原反应:有机物分子失氧得氢的反应。乙醇能被高锰酸钾酸性溶液氧化,乙醇能使高锰酸钾酸性溶液褪色。CH3CH2OHCH3CHOCH3COOH氧化氧化氧化氧化乙醇能被重铬酸钾酸性溶液氧化,乙醇能使重铬酸钾酸性溶液由橙黄色变为灰绿色。55、几种重要醇的性质和用途、几种重要醇的性质和用途⑴甲醇:有毒,工业酒精中含有甲醇不能饮用。⑵乙二醇和丙三醇(又称甘油):无色、粘稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。汽车用乙二醇防冻剂,丙三醇用于制造炸药,配制化妆品等。乙醇能不能被其他氧化剂氧化?实验3-2C—C—HHHHHO—H脱去两个氢与O结合成水乙醇在催化剂存在条件下被氧化时,乙醇分乙醇在催化剂存在条件下被氧化时,乙醇分子中哪些化学键发生断裂?子中哪些化学键发生断裂?写出下列各种醇在催化剂存在条件下被氧化写出下列各种醇在催化剂存在条件下被氧化而生成的化合物的结构简式。而生成的化合物的结构简式。OHCHCH22CHCH22CHCH22CHCH33OHCHCH33--CHCH--CHCH22CHCH33讨论:讨论:CHCH33CHCH22CHCH22CHOCHOOCHCH33--CC--CHCH22CHCH33CH3CH2OHCH3CHOCH3COOH[O][O]CH3CH2ONaCH3CH2BrCH2=CH2CH3CH2-O-CH2CH3乙醇的化学性质小结NaHBr浓H2SO4170℃浓H2SO4140℃CH3-C-O-CH2CH3ONaOHNaOH水溶液加热水溶液加热NaOHNaOH醇溶醇溶液,加热液,加热1.下列有关乙醇的物理性质的应用中不正确的是()A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子深”的说法2.在下列物质中,分别加入金属钠,不能产生氢气的是()A.苯B、蒸馏水C、无水酒精D、75%的酒精AA3、比较乙烷和乙醇的结构,下列说法错误的是()A.两个碳原子都以单键相连B.分子里都含有6个相同的氢原子C.乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼B44、、AA是一种含碳、氢、氧三种元素的有机化合物。已是一种含碳、氢、氧三种元素的有机化合物。已知:知:AA中碳的质量分数为中碳的质量分数为44.1%44.1%,氢的质量分数为,氢的质量分数为8.82%8.82%;;AA只含有一种官能团,且每个碳原子上最多只含有一种官能团,且每个碳原子上最多只连一个官能团:只连一个官能团:AA能与乙酸发生酯化反应,但不能能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请填空:在两个相邻碳原子上发生消去反应。请填空:AA的分子式是的分子式是,,其结构简式是其结构简式是。。CC55HH1212OO44--CC--HOHHOH22CCCHCH22OHOHCHCH22OHOHCHCH22OHOH----5、如何利用乙醇制备?CH2—CH2——OHOH浓硫酸170℃CH2=CH2↑+H2OCH3CH2OH│Br│BrCH2=CH2+Br2CH2-CH2+2NaOH│OH│OHCH2-CH2│Br│BrCH2-CH2+2NaBr什么是酚?羟基与芳香烃侧链上的碳原子相连,其化合物是芳香醇。羟基与苯环上的碳原子直接相连的化合物是酚。1、苯酚的结构二、酚二、酚常温下,苯酚能溶于水并能相互形成溶液(苯酚与水形成的浊液静置后会分层,上层是溶有苯酚的水层,下层是溶有水的苯酚层)⑴分子式:⑵结构简式:2、苯酚的物理性质(P52)-OH或C6H5OH苯酚有毒,它的浓溶液对皮肤有强烈的腐蚀性,使用时要小心,如不慎沾到皮肤上,应立即用酒精洗涤。注意C6H6O实验实验3-33-3完成下表中的实验,并填写实验现象。完成下表中的实验,并填写实验现象。液体呈浑浊液体呈浑浊液体由澄清透明变为浑浊液体由澄清透明变为浑浊液体由浑浊变为澄清透明液体由浑浊变为澄清透明现象现象实验实验⑴⑴向盛有少量苯酚晶体的试管向盛有少量苯酚晶体的试管中加入中加入2mL2mL蒸馏水,振荡试蒸馏水,振荡试管管⑶⑶再向试管中加入稀盐酸再向试管中加入稀盐酸⑵⑵向试管中逐滴加入向试管中逐滴加入5%5%的的NaOHNaOH溶液并振荡试管溶液并振荡试管3、苯酚的化学性质⑴苯酚的酸性受苯环的影响,酚羟基上的受苯环的影响,酚羟基上的HH比醇羟基上的比醇羟基上的HH活泼,酚羟基在水溶液中能够发生电离,显示酸性。活泼,酚羟基在水溶液中能够发生电离,显示酸性。-ONa+H2O(苯酚俗称石炭酸)(苯酚俗称石炭酸)+NaClNaClOH苯酚酸性比碳酸弱,比苯酚酸性比碳酸弱,比HCOHCO33强。强。--+NaHCONaHCO33OHONa+H2O+CO2ONa+HCl-OH+NaOH易溶于水易溶于水⑵苯酚的取代反应实验实验3-43-4向盛有少量苯酚稀溶液的试管里滴入过向盛有少量苯酚稀溶液的试管里滴入过量的浓溴水,观察现象。量的浓溴水,观察现象。有白色沉淀产生有白色沉淀产生实验现象:实验现象:受羟基的影响,苯基上的邻、对位的受羟基的影响,苯基上的邻、对位的HH变得更活泼了。变得更活泼了。苯酚与溴的反应很灵敏,常用于苯酚的定性检验苯酚与溴的反应很灵敏,常用于苯酚的定性检验和定量测定。和定量测定。⑵苯酚的取代反应OH+Br2OHBrBr--Br↓+HBr三溴苯酚,白色沉淀三溴苯酚,白色沉淀3333⑶⑶苯酚的显色反应苯酚的显色反应【【实验实验】】向盛有苯酚溶液的试管中滴入几滴向盛有苯酚溶液的试管中滴入几滴FeClFeCl33溶液,振荡,观察现象。溶液,振荡,观察现象。现象:现象:溶液呈紫色溶液呈紫色应用:检验苯酚的存在。应用:检验苯酚的存在。⑷⑷氧化反应氧化反应苯酚在空气中易被氧化而呈粉红色苯酚在空气中易被氧化而呈粉红色44、苯酚的用途:、苯酚的用途:P54P54P.54学与问1、苯和苯酚发生溴代反应的条件和产物有很大的不同。2、实验表明,苯酚的酸性比乙醇强。你如何从分子内基团间相互作用来解释下列事实。你如何从分子内基团间相互作用来解释下列事实。在苯酚的分子中,苯基影响了与其相连的羟在苯酚的分子中,苯基影响了与其相连的羟基上的氢原子,促使它比乙醇分子中羟基上的氢原子基上的氢原子,促使它比乙醇分子中羟基上的氢原子更容易电离;而羟基则反过来影响了与其相连的苯基更容易电离;而羟基则反过来影响了与其相连的苯基上的氢原子,使邻、对位上的氢原子更活泼,更容易上的氢原子,使邻、对位上的氢原子更活泼,更容易被其它的原子或原子团所取代。被其它的原子或原子团所取代。小结:



















